近日,上海科技大学物质科学与技术学院高得伟课题组首次实现了基于双环[1.1.0]丁烷(BCBs)衍生的硼酸酯复合物介导的1,2-金属盐重排反应,构建了一系列轴手性环丁烷硼酸酯。该工作解决了该类化合物在迁移反应时立体选择性难以调控的难题,为环丁烷手性化合物的合成提供了新的思路和方法,极大拓展该类化合物在手性化学中的应用空间。相关成果发表于国际学术期刊《自然-通讯》(Nature Communications)。
环丁烷骨架是有机化学中重要的单元,广泛存在于天然产物和生物活性分子中(图1a)。双环[1.1.0]丁烷(BCBs)及其衍生物由于桥连的C−C σ键具有高的环张力特性,近年来引起学术界的关注。该类化合物主要通过两种途径合成环丁烷骨架,其中之一就是BCB衍生的硼酸酯复合物通过1,2-金属酸盐重排反应,实现自由基或离子途径的环张力释放反应以制备多取代环丁烷硼酸酯(图1b)。可能是因为BCB衍生物的高反应活性使得反应的选择性调控极具挑战性(图1c),故其不对称调控一直进展缓慢。如果能够利用环张力释放策略,通过手性催化剂的精准调控,实现BCB硼酸酯复合物迁移反应的不对称控制,将显著拓展该类化合物在手性化学中的应用空间。
上海科技大学高得伟课题组致力于有机硼介导的新反应和新机制以及含硼药物化学的研究。本研究利用BCB衍生的硼酸酯复合物的高张力特性,诱导其发生1,2-迁移反应,并捕获体系中生成的匹配的二价钯非对映异构体,成功实现了一系列阻转异构环丁烷硼酸酯的高效不对称合成。值得一提的是,该过程中的动态动力学不对称转化顺利进行,对于实现高立体选择性起到了关键作用。此外,由于pinacol基团位阻效应和BCB的电子效应,导致迁移过程中形成的物种无法从endo面进攻钯(II)中间体,从而选择性地生成顺式环丁烷产物。目标产物中的C−B键将极大地促进后续的官能团转化,为构建轴手性环丁烷分子库提供了新的策略(图1d)。
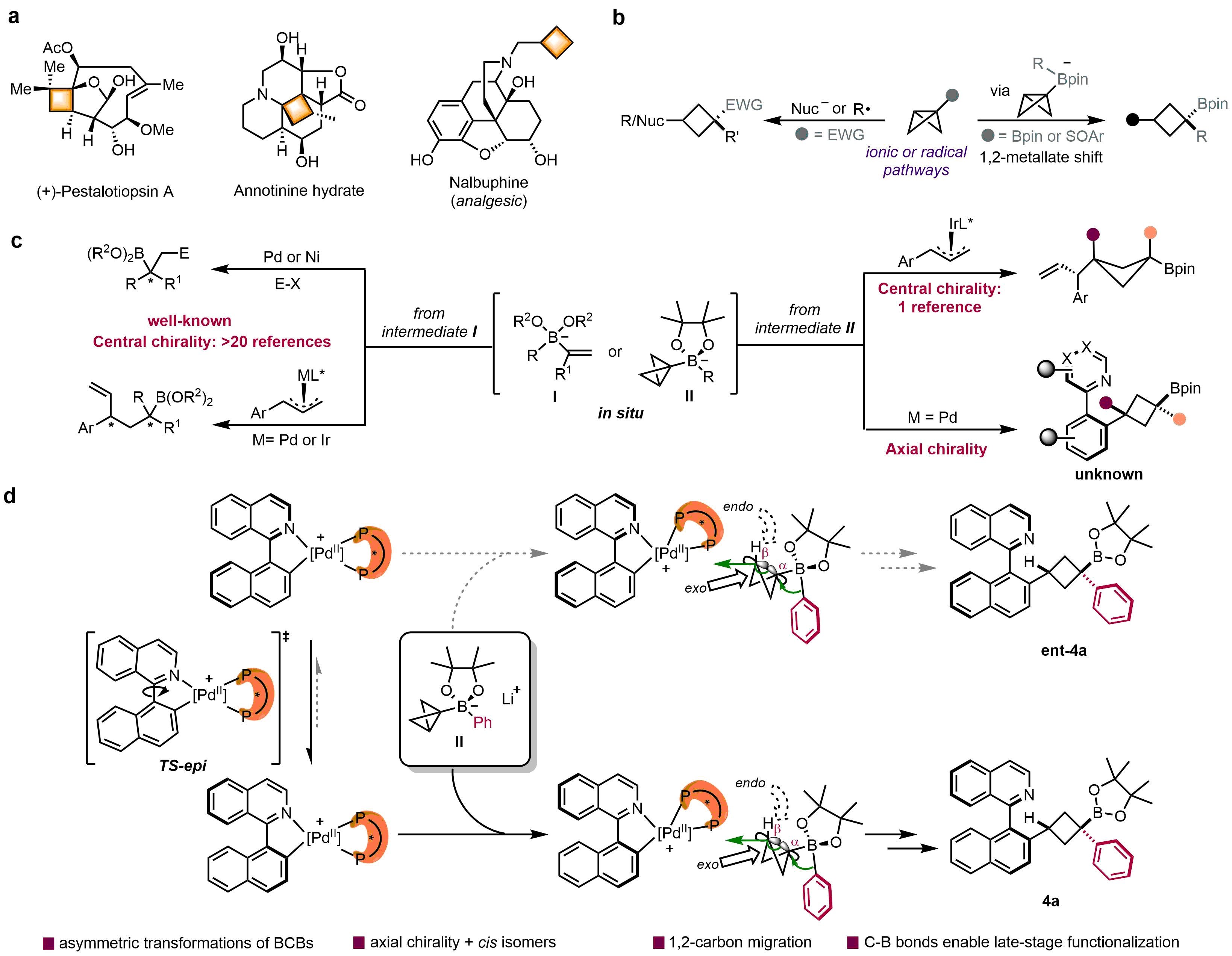
图1. 研究背景以及课题设想
进一步的反应机制研究发现,当使用(Ra)-L7作为手性配体时,能以43%的分离收率和91%的ee值得到目标产物4a。同时伴随着3a的分解副产物的生成,可能是由于体系中生成不匹配的Pd(II)中间体。当(Sa)-L7为手性配体时,可能是生成了匹配的Pd(II)中间体,反应能以83%的分离收率得到几乎光学纯的目标产物4a,且3a的分解得到了明显地抑制。当使用消旋配体时,也许因为两种配体的反应速度相差并不是特别大,反应以48%的收率和-15%的ee值得到目标产物4a,且产生了大量的副产物3a’(图2a)。最后,非线性效应研究表明在对映选择性决定步骤中金属和配体可能是1:1配位的(图2b)。
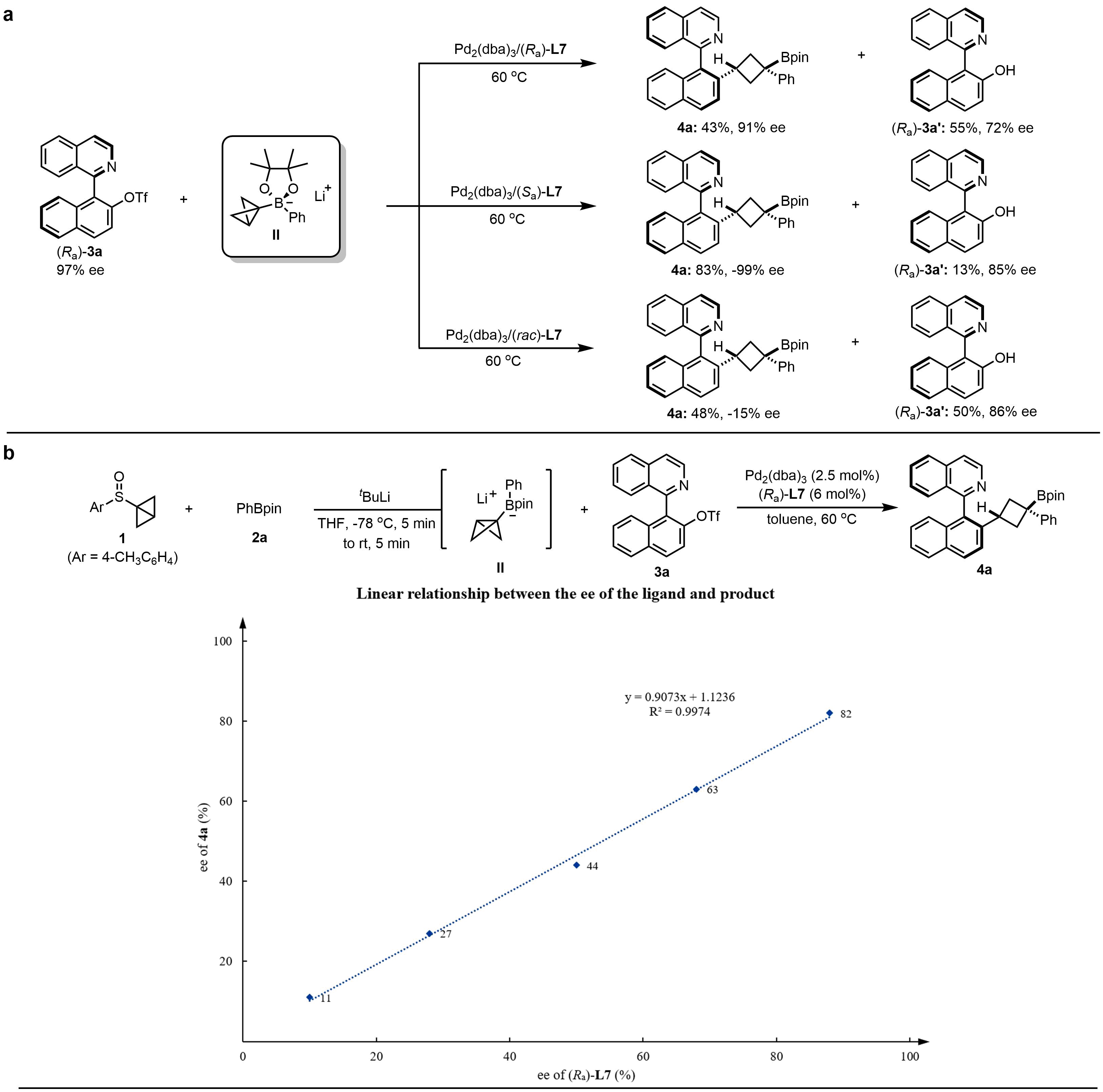
图2. 反应机理实验
上海科技大学博士研究生孙宇雯和上海工程技术大学硕士研究生赵家辉(上海科技大学访问生)为本文共同第一作者,上海科技大学高得伟教授与上海工程技术大学冯煌迪教授为本文的共同通讯作者,上海科技大学为第一完成单位。
论文标题:Asymmetric synthesis of atropisomers featuring cyclobutane boronic esters facilitated by ring-strained B-ate complexes


 沪公网安备 31011502006855号
沪公网安备 31011502006855号