近日,上海科技大学iHuman研究所/生命科学与技术学院水雯箐课题组与中国科学院上海药物研究所以及临港实验室多个研究团队开展合作,在《科学》(Science)期刊发表题为“Noncanonical agonist-dependent and -independent arrestin recruitment of GPR1”的研究论文。该工作在解析趋化素受体GPR1的功能调控机制方面取得突破性进展,首次阐明了阻遏蛋白(β-arrestins)调控GPR1信号的分子机制,拓展了对G蛋白偶联受体非典型信号转导与调控机制的理解。

趋化素是一类重要的脂肪因子,在脂质代谢、胰岛素敏感性以及免疫细胞迁移中发挥关键作用,是肥胖、糖尿病及代谢性炎症等疾病的重要潜在药物靶标。趋化素信号主要由两类受体共同介导:CMKLR1作为典型GPCR,主要依赖G蛋白信号通路驱动脂质代谢与炎症反应;而GPR1则属于非典型GPCR,主要通过β-arrestins介导信号,促进受体内吞,清除过量趋化素。趋化素系统通过这种“经典激活—非典型平衡”的双重机制,在代谢与炎症调控中发挥核心作用,但其结构基础与分子机制至今尚未明确。
研究团队利用单颗粒冷冻电镜技术,解析了GPR1在多种功能状态下与β-arrestins的复合物结构,包括与趋化素及β-arrestin 1或β-arrestin 2结合的形式,以及关键的无激动剂结合的GPR1–β-arrestin 1复合物。结果显示,在趋化素存在下,β-arrestin 1表现出显著的构象可塑性,其指状环(finger loop)与C-edge采用从“预结合”到“稳定结合”的多种结合模式,呈现出动态的招募过程。相比之下,β-arrestin 2与GPR1结合时,主要采取一种有助于受体内吞和信号转导的结合模式。
尤为重要的是,在不与趋化素结合时,GPR1的构象处于非激活态,但能通过一种全新的模式与β-arrestin1结合。鉴于GPCR信号传导中受体C末端的磷酸化修饰是招募β-arrestin的关键步骤,通过磷酸化质谱分析发现,GPR1的C端区域存在较高的本底磷酸化水平,且修饰位点形成一个独特的“磷酸化条形码”,这使得GPR1无需激动剂激活,即可预先具备β-arrestin识别的分子基础,从而促进受体对β-arrestin的招募,并启动受体内吞。
此外,脂质组亲和质谱分析发现,两种内源性脂肪酸(棕榈油酸和棕榈酸)可能通过介导非激活态GPR1与β-arrestin 1的结合,促进GPR1的自发性内吞,提示该类脂分子对于GPR1清除非激活型趋化素发挥调控作用。研究人员进一步检测脂肪细胞中的脂质含量,发现在高脂环境下CMKLR1促进脂肪代谢,降低了脂质积累,而GPR1通过清除非激活型趋化素促进CMKLR1激活,从而辅助脂质代谢。基于上述发现,研究团队提出了GPR1功能调控的“磷酸化编码-脂质辅助”模型:预先存在的磷酸化条形码负责启动识别,而内源性脂质则作为变构稳定剂巩固结合,二者协同确保了GPR1“清道夫”功能的高效执行。
这项研究首次揭示了GPR1作为“清道夫受体”的分子全貌,该受体通过阻遏蛋白偏向性信号和脂质辅助的内吞机制精细调控趋化素信号稳态。同时,提出了趋化素受体CMKLR1和GPR1对脂质代谢的协同调控机制。这些发现不仅拓展了对于GPCR信号转导机理的认识,也为肥胖、代谢性炎症等疾病的精准干预提供了新的线索和潜在靶点。
研究论文的第一作者包括临港实验室博士生蔡恒、国科大杭州高等研究院博士生林晓文、赵乐琛和副研究员何茂洲、上海科技大学生命科学与技术学院2023级博士生余洁和iHuman研究所副研究员张冰洁,以及中国科学院上海药物研究所博士生马元娣。中国科学院上海药物研究所吴蓓丽研究员、临港实验室朱亚研究员、中国科学院上海药物研究所赵强研究员、上海科技大学生命学院/iHuman研究所水雯箐教授与中国科学院上海药物研究所谢岑研究员为共同通讯作者。
论文链接: https://doi.org/10.1126/science.adt8794
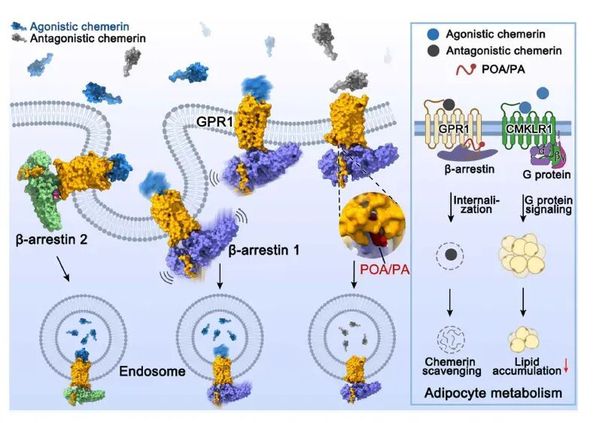
GPR1与阻遏蛋白的复合物结构示意图。趋化素受体GPR1在脂肪代谢和炎症反应中发挥重要作用,是肥胖和炎症的潜在药物作用靶点。图中GPR1与阻遏蛋白的不同的复合物结构用蛋白质表面图表示,GPR1为橙色,β-arrestin 1和β-arrestin 2分别为蓝色和绿色,激活型趋化素和非激活型趋化素分别为浅蓝色和灰色。(图片由中国科学院上海药物研究所吴蓓丽研究组提供)


 沪公网安备 31011502006855号
沪公网安备 31011502006855号