近日,上海科技大学物质科学与技术学院高得伟课题组发展了1,2-氧迁移驱动的双环[1.1.0]丁烷(BCB)硼酸酯不对称C–C σ键双官能团化反应,高效制备出手性顺式环丁烷硼酸酯衍生物。该工作突破了烷氧基金属盐活化有机硼酸酯时易发生转金属化的局限,为发展不对称1,2-氧迁移反应提供了新思路。相关成果发表于国际学术期刊《自然-通讯》(Nature Communications)。
有机硼酸酯是合成化学中重要的转化砌块,经典偶联反应通常利用烷氧基金属盐(ROLi,RONa或ROK等)来活化硼酸酯,经由转金属化过程、还原消除步骤来构筑C–C或C–X键。如能利用底物与催化剂的协同调控,抑制转金属化步骤,同时促进1,2-氧迁移反应的发生,将丰富基元反应类型,有助于发展新型有机合成反应。
多取代环丁烷广泛存在于具有抗菌、抗炎、抗肿瘤等活性的药物分子中,其环上取代基的种类、位置与构型直接决定药物的生物活性、代谢稳定性及靶向性,是药物分子设计优化的关键。双环[1.1.0]丁烷(BCB)环张力高、C–C σ键易断裂,是构建环丁烷骨架的理想前体。BCB硼酸酯(BCB-Bpin)兼具环张力的存在且C–B键易于后续转化,近来受到关注。目前报道的基于硼酸酯复合物的不对称迁移反应仅两例,且均局限于1,2-碳迁移反应。1,2-氧迁移一直鲜有报道,这是由于烷氧基盐活化硼酸酯后,不仅极易发生转金属化过程,且反应的立体化学难以精准调控,制约了其在合成化学等领域中的应用。
针对上述挑战,高得伟课题组利用烷氧基锂试剂与BCB-Bpin原位制备高活性的环张力硼酸酯复合物,结合BCB固有的环张力特性和配体调控手段,抑制竞争性的转金属化途径,并选择性地促进不对称1,2-氧迁移反应。上述过程需借助手性配体调节IrIII(π-烯丙基)中间体的异构化,使其能够被环张力硼酸酯复合物所捕获,经历独特的C–B键旋转以及1,2-氧迁移分步过程,最终实现了BCB中C–C σ键的碳烷氧基双官能团化反应,高效构建了多取代的顺式环丁烷硼酸酯(图1)。
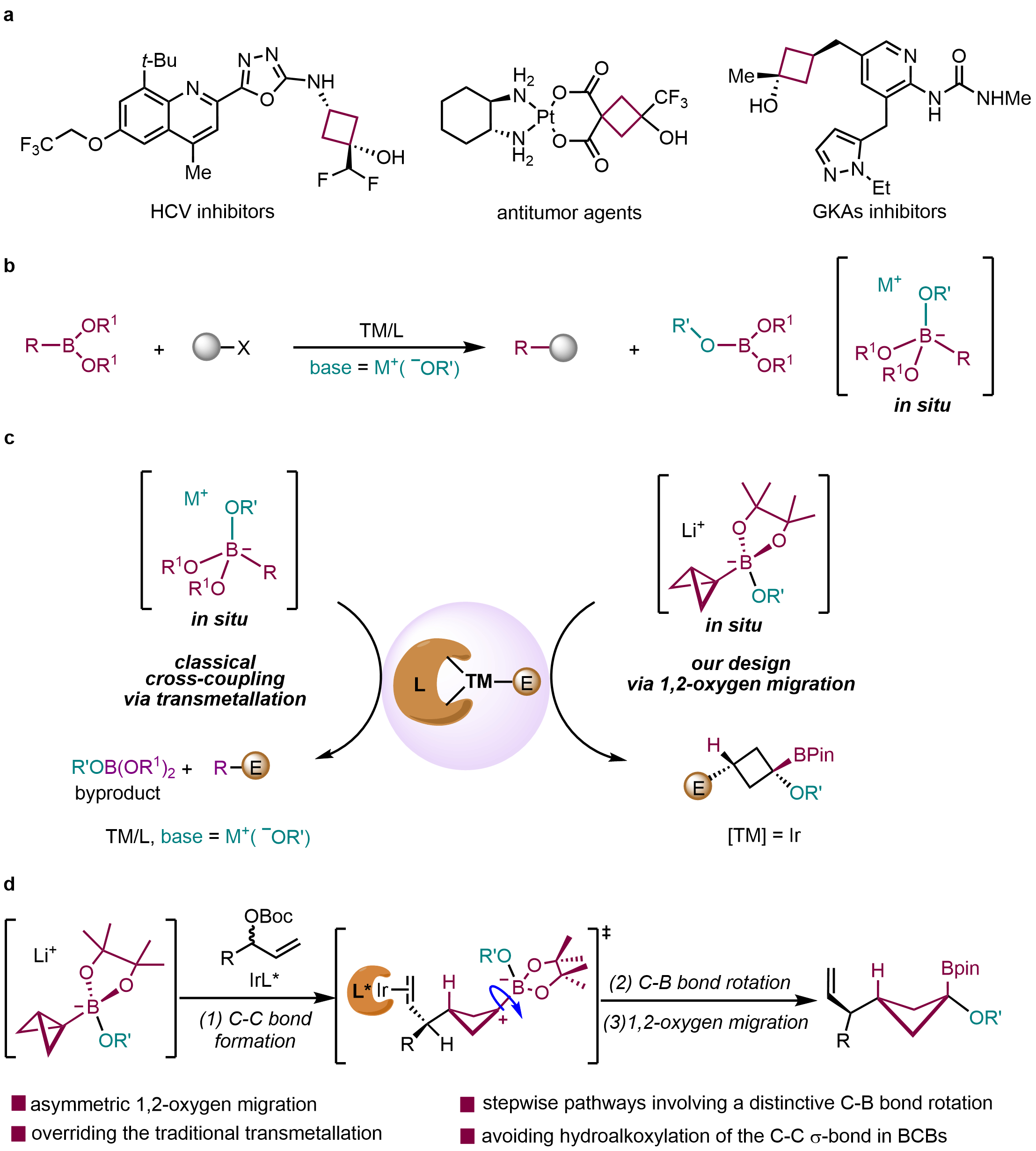
图1. 研究背景以及课题设想
研究人员通过一系列控制实验、非线性效应实验、动力学实验及哈米特方程研究,并结合密度泛函理论(DFT)计算,提出了该反应的可能机理(图2)。机理研究表明,反应遵循分步路径:首先发生C–C键形成,随后经历独特的C–B键旋转过程,最终进行1,2-氧迁移。其中,C–C键形成是整个反应的速率决定步骤,而C–B键旋转则是实现产物顺式选择性的关键步骤。
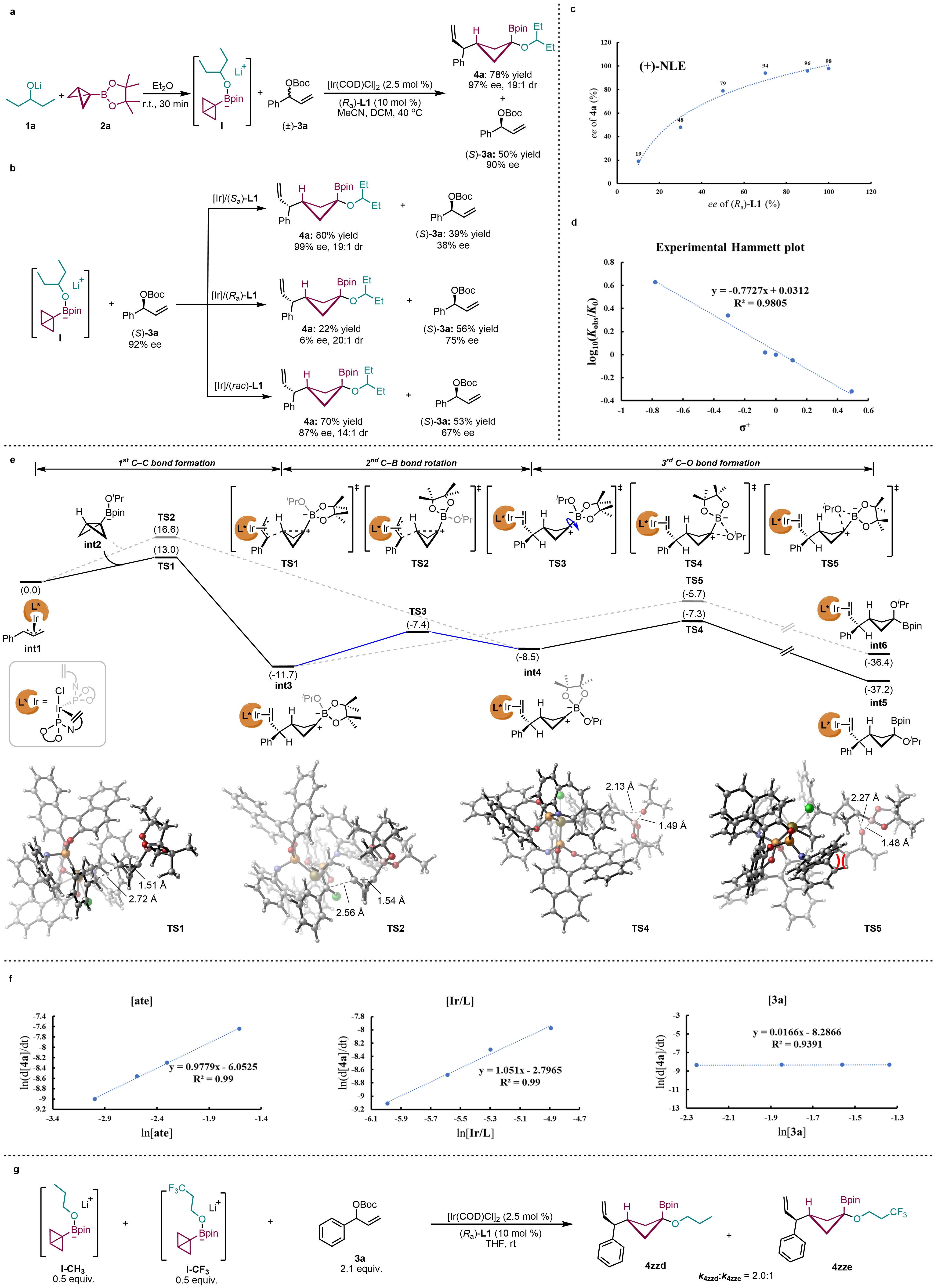
图2. 机理研究
上海科技大学博士研究生朱新愿为本文的第一作者,高得伟教授为通讯作者,上海科技大学为第一通讯单位。
论文标题:Catalytic Asymmetric Functionalization of Bicyclo[1.1.0]butane Boronic Esters Enabled by 1,2-Oxygen Migration


 沪公网安备 31011502006855号
沪公网安备 31011502006855号