近日,上海科技大学免疫化学研究所白芳课题组与中科苏州药物研究院梅良和团队合作,在《美国科学院院刊》(PNAS)在线发表题为“DeepDegradome: A Structure-Aware Deep Learning Framework for PROTAC and Ligand Generation Against Protein Targets”的研究论文,提出一种分子片段驱动、蛋白结构感知的药物设计算法框架,可实现小分子配体及其对应PROTAC(Proteolysis Targeting Chimera,蛋白降解靶向嵌合体)降解剂的从头设计,为药物研发提供了兼容多分子模态的自动化设计新工具。
靶向蛋白降解(TPD)特别是PROTAC技术,已成为药物研发的前沿方向。传统PROTAC设计多局限于在已知配体间优化连接子,难以突破既有分子骨架,尤其对缺乏明确结合口袋的“难成药”靶标很难实现理性设计。基于片段的药物设计(FBDD)虽可通过组装低分子量片段探索广阔化学空间,但其实验流程依赖高灵敏度生物物理方法,限制了规模化应用。为解决这一瓶颈,本研究开发了DeepDegradome——首个基于FBDD将小分子配体与PROTAC设计统一于结构感知框架的AI生成模型。
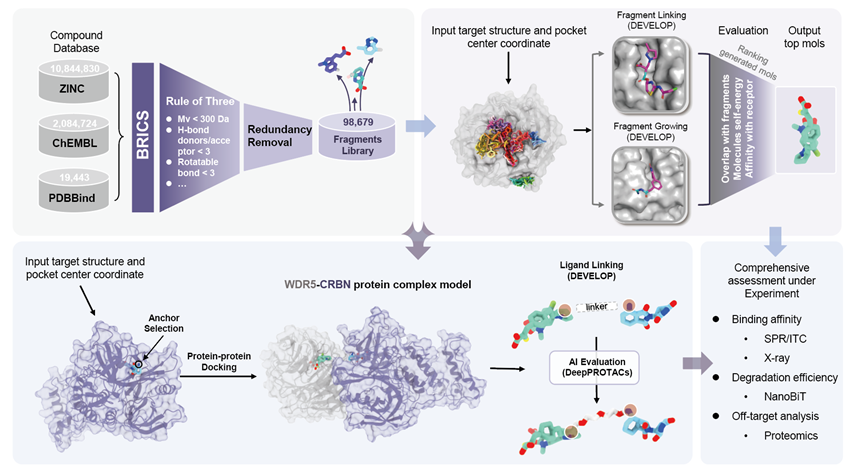
图一:DeepDegradome模型的整体框架
DeepDegradome的核心流程(图一)涵盖分子片段构建、靶标结构解析、分子生成与性能评估等关键环节。首先,研究团队利用分子片段拆分算法对ZINC、ChEMBL、PDBBind等公共数据库中的类药分子进行系统分解,构建包含约10万个结构多样的分子片段库;随后,基于课题组自主开发基于多目标优化的分子对接算法iFitDock,对靶标潜在结合口袋开展全局扫描,识别具有设计潜力的“可药性亚口袋”,并对潜在高亲和力片段进行聚类与综合评价。在此基础上引入图神经网络(GNN),结合受体微环境的药效特征信息,通过“片段连接”与“片段生长”策略,将分布于不同亚区域的优势片段智能组装为完整候选分子,并通过三维构象叠合、配体应变能评估及结合亲和力预测等多维度筛选,确保其兼具合理结合模式与优良结合性能。在PROTAC设计场景中,DeepDegradome引入蛋白质–蛋白质互作模式作为空间约束依据,围绕互作界面的构象距离特征开展连接子生成与优化,最终实现PROTAC分子的从头设计。最终结合课题组自主研发的深度学习降解药效预测模型DeepPROTACs进行综合评价与筛选,形成覆盖结构建模、分子生成到降解效能评估的一体化智能设计流程。
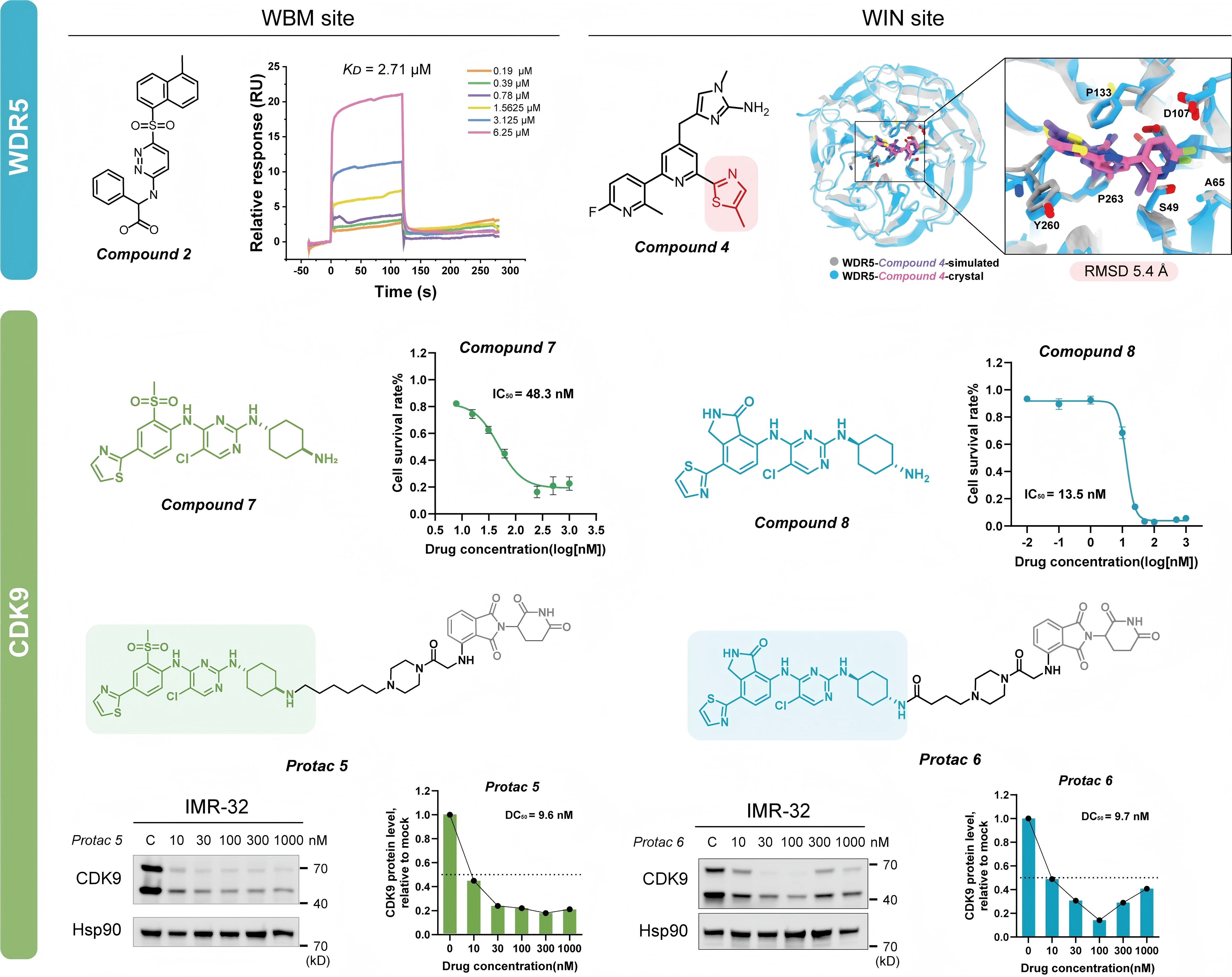
图二:DeepDegradome靶向WDR5与CDK9开展PPI阻断剂和PROTAC生成应用示例
为验证DeepDegradome的有效性,研究团队选取染色质相关蛋白WDR5(缺乏典型药物结合口袋的难成药靶标)和激酶CDK9(经临床验证的抗癌靶标)开展化合物生成与应用研究,相关候选分子由梅良和团队完成合成。分别针对WDR5与不同蛋白质互作的WIN位点和WBM位点,DeepDegradome生成了多个结构新颖的小分子配体,其中化合物2与WDR5的结合亲和力(Kd)达2.71μM,且能有效破坏WDR5-MYC相互作用;化合物4的预测结合构象与后续解析的晶体结构高度吻合(RMSD 5.4 Å),证实了模型在三维构象生成中的准确性。针对CDK9,模型生成的化合物7和化合物8在IMR-32神经母细胞瘤细胞中展现出纳摩尔级的抗增殖活性(IC50分别为48.3nM和13.5nM),并浓度依赖性地抑制下游POLR2A CTD磷酸化及N-MYC表达。进一步将化合物7和8与CRBN配体泊马度胺通过不同连接子偶联,所得PROTAC分子(Protac 3-6)在细胞内诱导CDK9降解的DC50最低可达9.6 nM,最大降解效率超过85%。在与其他生成模型的基准比较中,DeepDegradome在生成成功率、对接亲和力、分子键长键角分布等方面均表现最优,生成的分子在类药性和结构新颖性之间取得了良好平衡。综上,本研究为靶向蛋白降解技术提供了可扩展、高可靠的计算工具,有望加速新型降解剂的发现进程。
课题组目前已经形成从PROTAC数据库构建、从头分子生成、连接子生成、降解药效评价、可合成性评价、靶向EGFR的PROTAC分ADMET预测等系列工作,形成完善的PROTAC药物设计计算方法,为靶向难成药靶标的降解剂类药物设计提供了系统的技术支持。
上海科技大学免疫化学研究所原博士后胡乔宇、生命科学与技术学院2023级博士研究生曹宇和2021级博士研究生任鹏璇(现山西医科大学讲师)为论文共同第一作者。胡乔宇、梅良和和上海科技大学免疫化学研究所研究员、生命科学与技术学院副教授白芳为论文共同通讯作者。上海科技大学为第一完成单位。
文章信息:DeepDegradome: A Structure-Aware Deep Learning Framework for PROTAC and Ligand Generation Against Protein Targets,Qiaoyu Hu, Yu Cao, PengXuan Ren, Xianglei Zhang, Fenglei Li, Xueyuan Zhang, Fengyu Cai, Ran Zhang, Yongqi Zhou, Lianghe Mei, and Fang Bai. Proc. Nat. Acad. Sci. USA., 2026, DOI:10.1073/pnas.2518248123
文章链接:https://doi.org/10.1073/pnas.2518248123


 沪公网安备 31011502006855号
沪公网安备 31011502006855号