近日,上海科技大学物质科学与技术学院李健课题组在人工酶设计领域取得新进展,以转录调控蛋白LmrR为工程化骨架,创新构建出一种基于N端天然脯氨酸的人工醛缩酶,实现了高对映选择性的醛缩生物催化反应,为开发“new-to-nature”非天然生物催化剂提供了新的设计思路和理论基础。相关成果在线发表于国际学术期刊《自然-通讯》(Nature Communications)。
不对称醛缩反应是构建手性碳–碳键的核心方法,在药物分子和精细化学品合成中具有重要意义。传统的L-脯氨酸有机小分子催化已被广泛应用,但在水相条件下稳定性有限,且难以通过遗传手段优化。近年来,研究人员尝试将有机催化机理“移植”进蛋白内部,打造具备新功能的人工酶。然而,大多数策略依赖非天然氨基酸或化学修饰,限制了体系的可扩展性和生物兼容性。为突破上述限制,李健课题组提出了一种全新的设计理念,仅利用天然氨基酸(L-脯氨酸),通过对蛋白序列与结构的理性改造,在蛋白内部构建具有有机催化活性的中心。
本研究选择细菌转录调控蛋白LmrR作为工程化骨架,LmrR由同源二聚体形成一个较大的疏水性内腔,为底物结合与催化提供了良好的结构基础。通过精细的结构设计,将一个天然L-脯氨酸残基重新定位为蛋白质的N端,嵌入疏水腔体内部,使其成为能够进行烯胺催化的活性中心,成功构建了基于N端L-脯氨酸的人工醛缩酶(图1)。通过对反应条件优化和底物拓展研究,该人工酶在不对称醛缩反应中可实现超过99%的底物转化率与对映选择性,并对多种芳香醛底物展现出优异的催化效率和立体控制能力(图2)。
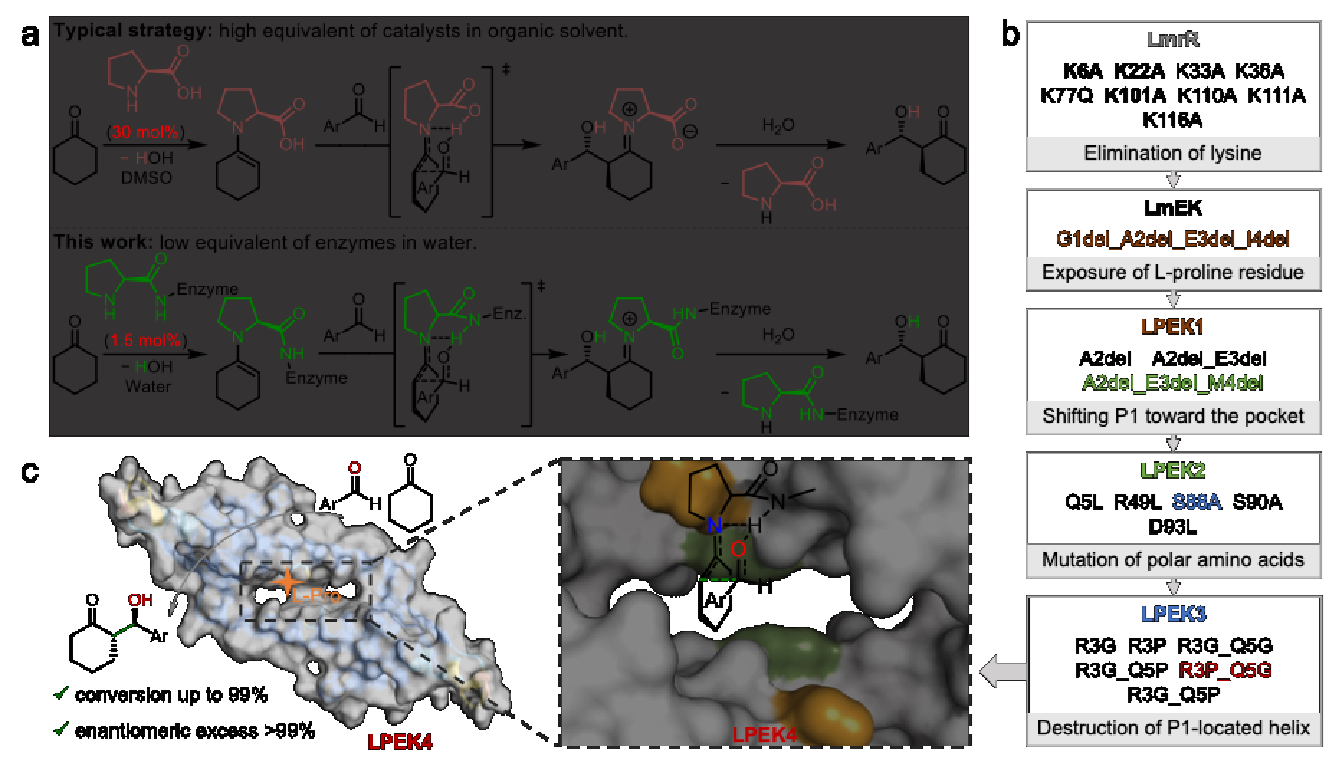
图1 基于LmrR的人工醛缩酶设计,实现高对映选择性生物催化反应。
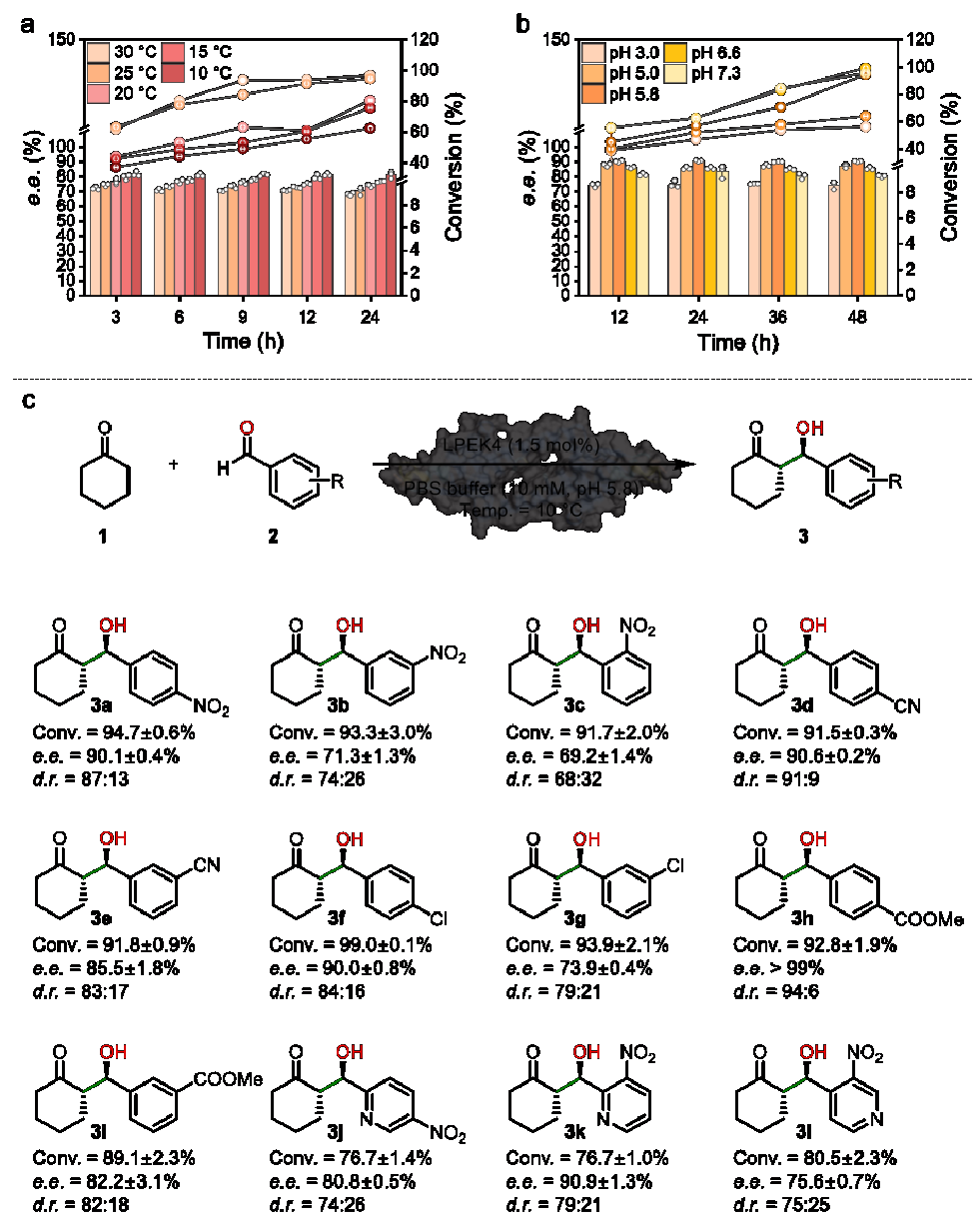
图2 人工醛缩酶的反应条件优化及底物谱测试。
本研究提出了一种全基因编码、无需引入非天然组分的人工酶设计新路径,为人工酶的理性设计与后续定向进化提供了稳定、可扩展的平台,也为有机催化与生物催化的深度融合奠定了重要理论与实践基础。
上海科技大学物质科学与技术学院李健课题组博士后卢皓凡为论文第一作者,李健教授为通讯作者。上海科技大学为第一完成单位,先进医用材料与医疗器械全国重点实验室和上海临床研究中心为论文共同完成单位。
论文标题:Engineering LmrR protein for L-proline-based asymmetric aldol biocatalysis


 沪公网安备 31011502006855号
沪公网安备 31011502006855号